Isotopes
Les isotopes sont des atomes d'un même élément chimique qui ont donc le même nombre de protons, mais qui diffèrent par leur nombre de neutrons et donc par leur masse.
Exemple : l'uranium 235 et l'uranium 238 dont le premier a 143 neutrons et le deuxième, 146 neutrons.
1. Les isotopes
étymologie : ISOS : (grec) même, identique / TOPOS : lieu
définition : Isotope signifie par étymologie : même lieu. Ce sont en effet des éléments chimiques qui se retrouvent dans la même case que d'autres dans le tableau périodique, car ils possèdent les mêmes propriétés chimiques que l'élément qui le représente.
La seule différence entre les isotopes d'un même élément se trouve au niveau du nombre de nucléons (particules) composant leur noyau. C'est le nombre de neutrons, particules neutres qui varie selon les isotopes.Les isotopes sont caractérisés par leur nombre de masse A correspondant au nombre de nucléons, c'est-à-dire la somme du nombre de protons et de neutrons présents dans le noyau. Il est toujours indiqué en haut à gauche du symbole de l'isotope.
· C'est le nombre de protons qui détermine l'élément, le nombre de neutrons n'intervient pas. Un atome dont le noyau est composé de 3 protons est un atome de lithium, et reste un atome de lithium avec 1, 2 ou 3 neutrons.
· Pour les différents isotopes d'un élément, le nombre de protons est identique, seul le nombre de neutrons varie.
· Plus un isotope possède des neutrons, plus sa masse augmente (plus il est lourd). En effet la masse du neutron est pratiquement équivalente à la masse d'un proton.
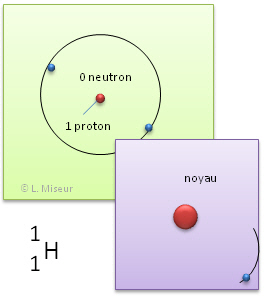
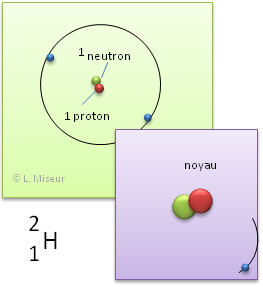
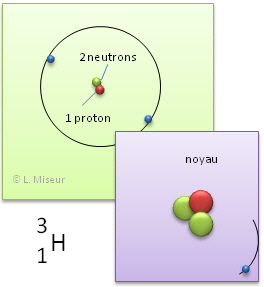
Exemple: l'hydrogène. Il existe d'autres atomes qui ont les mêmes propriétés chimiques que l'élément hydrogène. Ils ont le même nombre de protons et d'électrons, mais leurs nombres de neutrons sont différents.
Exemple : l'uranium 235 et l'uranium 238 dont le premier a 143 neutrons et le deuxième, 146 neutrons.
1. Les isotopes
étymologie : ISOS : (grec) même, identique / TOPOS : lieu
définition : Isotope signifie par étymologie : même lieu. Ce sont en effet des éléments chimiques qui se retrouvent dans la même case que d'autres dans le tableau périodique, car ils possèdent les mêmes propriétés chimiques que l'élément qui le représente.
La seule différence entre les isotopes d'un même élément se trouve au niveau du nombre de nucléons (particules) composant leur noyau. C'est le nombre de neutrons, particules neutres qui varie selon les isotopes.Les isotopes sont caractérisés par leur nombre de masse A correspondant au nombre de nucléons, c'est-à-dire la somme du nombre de protons et de neutrons présents dans le noyau. Il est toujours indiqué en haut à gauche du symbole de l'isotope.
· C'est le nombre de protons qui détermine l'élément, le nombre de neutrons n'intervient pas. Un atome dont le noyau est composé de 3 protons est un atome de lithium, et reste un atome de lithium avec 1, 2 ou 3 neutrons.
· Pour les différents isotopes d'un élément, le nombre de protons est identique, seul le nombre de neutrons varie.
· Plus un isotope possède des neutrons, plus sa masse augmente (plus il est lourd). En effet la masse du neutron est pratiquement équivalente à la masse d'un proton.
Exemple: l'hydrogène. Il existe d'autres atomes qui ont les mêmes propriétés chimiques que l'élément hydrogène. Ils ont le même nombre de protons et d'électrons, mais leurs nombres de neutrons sont différents.
Ces atomes ont les mêmes propriétés chimiques. En effet, ces propriétés sont déterminées par le nombre d'électrons et celui-ci reste identique. ATTENTION ! Ces atomes n'ont pas les mêmes propriétés physiques (leur masse est déjà différente).
Les isotopes sont naturels (présents dans la nature) ou artificiels (fabriqués dans les laboratoires et industriels - ex. : technétium 99 utilisé en scintigraphie).
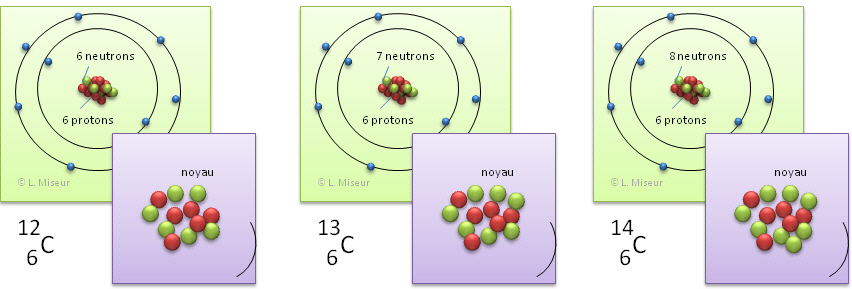
2. Les isotopes du carbone
Il existe 3 isotopes pour le carbone : ¹²C, ¹³C, ¹⁴C, respectivement avec un noyau composé de 6 neutrons, 7 neutrons et 8 neutrons.
Les isotopes sont naturels (présents dans la nature) ou artificiels (fabriqués dans les laboratoires et industriels - ex. : technétium 99 utilisé en scintigraphie).
2. Les isotopes du carbone
Il existe 3 isotopes pour le carbone : ¹²C, ¹³C, ¹⁴C, respectivement avec un noyau composé de 6 neutrons, 7 neutrons et 8 neutrons.
Radioactivité :
Un des isotopes du Carbone est particulièrement célèbre !
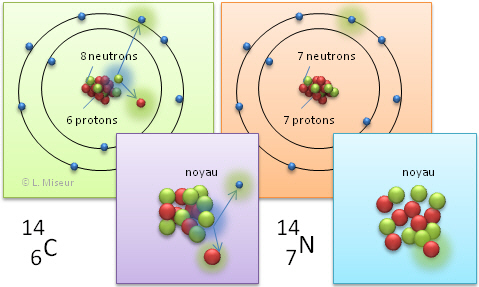
Tu as certainement déjà entendu parler du carbone "14". Il s'agit d'un isotope du carbone dont le noyau est composé de 14 nucléons : 6 protons et 8 neutrons.
Cet isotope du carbone n'est pas stable dans le temps. Il est radioactif. C'est à dire qu'il se désintègre petit à petit en émettant des radiations. Mais il a les mêmes propriétés chimiques que le carbone 12 (l'isotope le plus courant du Carbone), même s'il est un peu plus lourd. Donc le carbone 14 peut entrer dans la composition de n'importe quel être vivant.
Les scientifiques ont déterminé un temps de demi-vie (appelé la période radioactive) pour le carbone 14. C'est le temps que met une masse de carbone 14 pour être désintégrée en azote et réduite de moitié.
Le temps de demi vie du ¹⁴C est de 5580 ans avec une marge d'erreur de +/- 30 ans, donc si l'on stocke 60 g de cet isotope radioactif, après 5580 ans, il n'en restera plus que 30g, le reste s'étant désintégré en atomes d'azote et en électrons.
Un des isotopes du Carbone est particulièrement célèbre !
Tu as certainement déjà entendu parler du carbone "14". Il s'agit d'un isotope du carbone dont le noyau est composé de 14 nucléons : 6 protons et 8 neutrons.
Cet isotope du carbone n'est pas stable dans le temps. Il est radioactif. C'est à dire qu'il se désintègre petit à petit en émettant des radiations. Mais il a les mêmes propriétés chimiques que le carbone 12 (l'isotope le plus courant du Carbone), même s'il est un peu plus lourd. Donc le carbone 14 peut entrer dans la composition de n'importe quel être vivant.
Les scientifiques ont déterminé un temps de demi-vie (appelé la période radioactive) pour le carbone 14. C'est le temps que met une masse de carbone 14 pour être désintégrée en azote et réduite de moitié.
Le temps de demi vie du ¹⁴C est de 5580 ans avec une marge d'erreur de +/- 30 ans, donc si l'on stocke 60 g de cet isotope radioactif, après 5580 ans, il n'en restera plus que 30g, le reste s'étant désintégré en atomes d'azote et en électrons.
Le carbone et ses différents isotopes est naturellement présent dans l'atmosphère et est capté par les organismes qui le stocke durant toute leur vie. Une fois l'organisme mort, les quantités de carbone accumulées ne sont plus renouvelées et l'isotope 14 du carbone se désintègre sans être remplacé.
En résumé, certaines isotopes, naturels ou artificiels, sont instables. Ils peuvent alors se désintégrer en émettant des rayonnements. On dit alors qu'ils sont radioactifs. Les isotopes radioactifs sont parfois appelés radio-isotopes.
Un élément chimique comprend souvent un ensemble d'isotopes caractérisés par le même numéro atomique Z mais possédant un nombre de masse A différent. Ces isotopes sont présents dans l'élément en proportions bien définies appelés "abondances".
Exemples :
35 37
Cl 75,77 % et Cl 24,23 %
17 17
En résumé, certaines isotopes, naturels ou artificiels, sont instables. Ils peuvent alors se désintégrer en émettant des rayonnements. On dit alors qu'ils sont radioactifs. Les isotopes radioactifs sont parfois appelés radio-isotopes.
Un élément chimique comprend souvent un ensemble d'isotopes caractérisés par le même numéro atomique Z mais possédant un nombre de masse A différent. Ces isotopes sont présents dans l'élément en proportions bien définies appelés "abondances".
Exemples :
35 37
Cl 75,77 % et Cl 24,23 %
17 17