Les liaisons chimiques
La liaison chimique est le phénomène physique qui lie les atomes entre eux en échangeant ou partageant un ou plusieurs électrons ou par des forces électrostatiques.
Pour rejoindre la stabilité des gaz rares, les atomes peuvent mettre en commun des électrons périphériques. Les atomes ainsi liés constituent des molécules et se trouvent dans une situation énergétique plus stable. Pour assurer la grande diversité des composés chimiques, des liens doivent se créer entre atomes de même espèce ou entre atomes différents : il convient donc de s'initier aux propriétés de la liaison chimique pour comprendre les réactions et leur déroulement. On a coutume de distinguer 3 grandes classes de liaisons chimiques fortes, c'est-à-dire stables :
* La liaison ionique
* La liaison covalente
* La liaison métallique
Nous verrons l'arrangement dans l'espace des atomes réunis par les liaisons, ce qui aboutit à décrire la géométrie des molécules et des agrégats ioniques. Nous les appellerons les liaisons intramoléculaires dont l'Energie de liaison = +/- 100 kcal/mol.
Un autre type de liaison : les liaisons intermoléculaires permettent la cohésion des molécules entre elles. Ces liaisons sont beaucoup plus faibles et leur énergie de liaison est petite par rapport aux liaisons intramoléculaires, soit E₁ = +/- 10 kcal/mol.
On distingue les forces de Van der Waals et les liaisons par pont hydrogène.
1. Les liaisons intramoléculaires
(dans la molécule X - Y - Z)
Les atomes caractérisés par un Z > 4 tendent à posséder 8 électrons sur leur couche périphérique, afin d'acquérir un état stable.
Exemple : molécule d'O ou les 2 atomes d'oxygène possèdent chacun 8 électrons sur leurs couche périphérique.
! Limite du modèle de l'octet !
Cette règle souffre de nombreuses exceptions : Certains atomes peuvent posséder plus de 8 électrons sur leur couche périphérique et d'autres tomes moins de 8 électrons ! La règle de l'octet ne s'applique strictement qu'aux atomes de la 2ème période qui ne peuvent posséder qu'au maximum 8 électrons sur leur dernière couche L.
Par contre, un atome de la 3ème période peut posséder :
* soit jusqu'à 18 électrons sur sa couche M → cas du phosphore, exemple : PCl₅.
* soit moins de 8 électrons autour de lui → cas du bore, exemple : H₃BO₃.
1.1. La liaison ionique
Elle résulte de l'attraction électrostatique entre ions de signes contraires. En général, la liaison ionique s'établit entre les atomes métalliques donneurs d'électrons des familles Ia, IIa et IIIa et les atomes non métalliques accepteurs d'électrons des familles VIa et VIIa.
Pour rejoindre la stabilité des gaz rares, les atomes peuvent mettre en commun des électrons périphériques. Les atomes ainsi liés constituent des molécules et se trouvent dans une situation énergétique plus stable. Pour assurer la grande diversité des composés chimiques, des liens doivent se créer entre atomes de même espèce ou entre atomes différents : il convient donc de s'initier aux propriétés de la liaison chimique pour comprendre les réactions et leur déroulement. On a coutume de distinguer 3 grandes classes de liaisons chimiques fortes, c'est-à-dire stables :
* La liaison ionique
* La liaison covalente
* La liaison métallique
Nous verrons l'arrangement dans l'espace des atomes réunis par les liaisons, ce qui aboutit à décrire la géométrie des molécules et des agrégats ioniques. Nous les appellerons les liaisons intramoléculaires dont l'Energie de liaison = +/- 100 kcal/mol.
Un autre type de liaison : les liaisons intermoléculaires permettent la cohésion des molécules entre elles. Ces liaisons sont beaucoup plus faibles et leur énergie de liaison est petite par rapport aux liaisons intramoléculaires, soit E₁ = +/- 10 kcal/mol.
On distingue les forces de Van der Waals et les liaisons par pont hydrogène.
1. Les liaisons intramoléculaires
(dans la molécule X - Y - Z)
Les atomes caractérisés par un Z > 4 tendent à posséder 8 électrons sur leur couche périphérique, afin d'acquérir un état stable.
Exemple : molécule d'O ou les 2 atomes d'oxygène possèdent chacun 8 électrons sur leurs couche périphérique.
! Limite du modèle de l'octet !
Cette règle souffre de nombreuses exceptions : Certains atomes peuvent posséder plus de 8 électrons sur leur couche périphérique et d'autres tomes moins de 8 électrons ! La règle de l'octet ne s'applique strictement qu'aux atomes de la 2ème période qui ne peuvent posséder qu'au maximum 8 électrons sur leur dernière couche L.
Par contre, un atome de la 3ème période peut posséder :
* soit jusqu'à 18 électrons sur sa couche M → cas du phosphore, exemple : PCl₅.
* soit moins de 8 électrons autour de lui → cas du bore, exemple : H₃BO₃.
1.1. La liaison ionique
Elle résulte de l'attraction électrostatique entre ions de signes contraires. En général, la liaison ionique s'établit entre les atomes métalliques donneurs d'électrons des familles Ia, IIa et IIIa et les atomes non métalliques accepteurs d'électrons des familles VIa et VIIa.
Le Cl étant plus électronégatif que le Na, attire l'électron de valence du Na afin de réaliser l'octet périphérique.
- L'atome de Na perd un électron et devient l'ion Na⁺ afin de réaliser également l'octet périphérique.
- L'atome Cl gagne un électron et devient ainsi l'ion Cl⁻.
Les ions Na⁺ et Cl⁻ ainsi formés, étant de signes contraires, s'attirent mutuellement par attraction électrostatique et forment une liaison ionique.
Cette liaison intervient lorsque la différence d'électronégativité est très grande (∆𝔁 > 1,8), la paire électronique est totalement déplacée vers l'atome le plus électronégatif.
Définition : la liaison ionique représente une attraction électrostatique entre ions formés par transfert d'électrons provenant d'atome d'électronégativité très différente.
Conséquences :
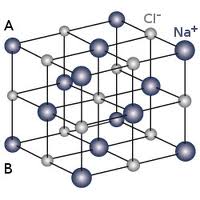
* Les corps ioniques forment des solides ioniques constitués par une alternance d'ions positifs et négatifs.
* Les forces de cohésion entre les ions (forces électrostatiques) sont très importantes, ce qui explique que la plupart des composés ioniques sont solides à température ordinaire.
Schéma d'un solide ionique :
- L'atome de Na perd un électron et devient l'ion Na⁺ afin de réaliser également l'octet périphérique.
- L'atome Cl gagne un électron et devient ainsi l'ion Cl⁻.
Les ions Na⁺ et Cl⁻ ainsi formés, étant de signes contraires, s'attirent mutuellement par attraction électrostatique et forment une liaison ionique.
Cette liaison intervient lorsque la différence d'électronégativité est très grande (∆𝔁 > 1,8), la paire électronique est totalement déplacée vers l'atome le plus électronégatif.
Définition : la liaison ionique représente une attraction électrostatique entre ions formés par transfert d'électrons provenant d'atome d'électronégativité très différente.
Conséquences :
* Les corps ioniques forment des solides ioniques constitués par une alternance d'ions positifs et négatifs.
* Les forces de cohésion entre les ions (forces électrostatiques) sont très importantes, ce qui explique que la plupart des composés ioniques sont solides à température ordinaire.
Schéma d'un solide ionique :
Propriété des composés ioniques : solides, formes particulières (maille), durs, se fragmentent nettement, température de fusion importante.
Exemples : Al₂O₃ : papier émeri, CaCO₃ : marbre, Al₂O₃ + Cr₂O₃ : rubis, MgO : brique réfractaire.
Remarque : la limite ∆𝔁 > 1,8 est arbitraire. Tous les corps où la ∆𝔁 est proche de 1,8 possèdent des liaisons partiellement ioniques et partiellement covalentes.
1.2. Les liaisons covalentes
La liaison covalente résulte de la mise en commun de 2 électrons.
a. Liaison covalente normale parfaite.
- normale : il s'agit d'une mise en commun de 2 électrons CÉLIBATAIRES.
- parfaite : entre 2 atomes de même électronégativité.
H . + . H ⇒ H - H
Liaison H₂ : Dans la molécule de Dihydrogène H₂, chaque atome H. met son électron célibataire en commun avec l'électron célibataire de l'autre atome. Chaque atome possède ainsi la même structure que le gaz rare He avec 2 électrons sur le niveau K (couche complète).
Définition : La Covalence Normale Parfaite est une mise en commun d'électrons célibataires entre atomes de même électronégativité (∆𝔁 ≈ 0)
Ce type de liaison donne toujours des molécules non polaires, très peu liées les unes aux autres.
b. Liaison covalente polarisée.
- normale : résulte de la mise en commun de deux électrons célibataires.
- polarisée : entre deux atomes d'électronégativité DIFFÉRENTE. Ceci a pour conséquence de faire apparaître une charge partielle sur chaque atome. ATTENTION : ma somme algébrique des charges partielles dans toute molécule est égale à zéro.
La flèche au milieu de la barre de liaison indique vers lequel des 2 atomes les &électrons de liaison sont attirés préférentiellement.
Lorsque 0,4 < ∆𝔁⁻ < 1,8, la paire électronique de la liaison est déplacée vers l'atome le plus électronégatif.
H. .Cl ⇒
Définition : La liaison covalente polarisée est une mise en commun de 2 électrons célibataires entre 2 atomes d'électronégativité différente. La liaison est polarisée vers l'atome le plus électronégatif.
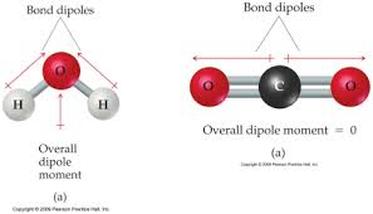
Les molécules obtenues de cette manière peuvent être polaires (la résultante des charges négatives ne coïncident pas avec la résultante des charges positives) ou non polaires selon la disposition des atomes à l'intérieur de la molécule.
Les molécules obtenues de cette manière peuvent être polaires (la résultante des charges négatives ne coïncident pas avec la résultante des charges positives) ou non polaires selon la disposition des atomes à l'intérieur de la molécule.
La molécule est polaire, c'est un dipôle La molécule est non polaire car la distribution des charges est symétrique.
c. Chimie organique et corps covalents
c. Chimie organique et corps covalents