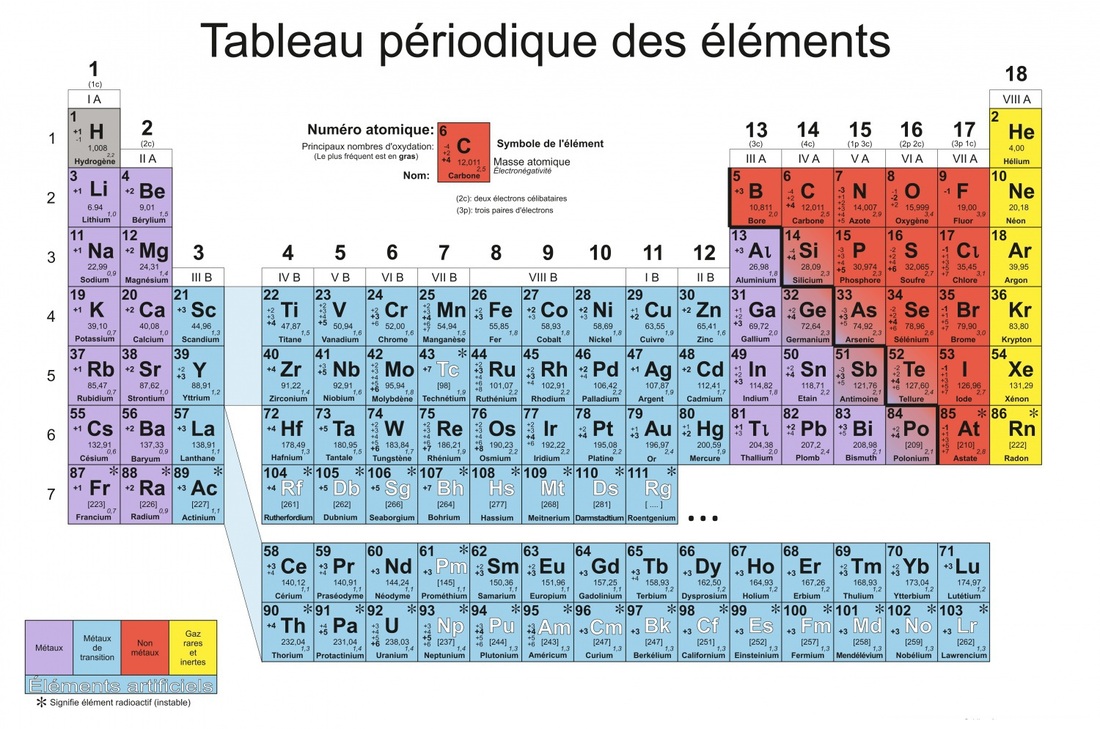
Tableau périodique
1. Dimitri Mendeleïev
Chimiste russe, il proposa le premier en 1869 la classification la plus élaborée et la plus complète des 66 éléments chimiques connus à l'époque.
Il classa les éléments par ordre croissant de leur masse atomique en allant à la ligne de telle sorte que les atomes ayant des propriétés semblables se trouvent l'un en dessous de l'autre, formant ainsi une famille.
2. Structure générale
- 7 lignes appelées les 7 PÉRIODES
Le numéro de la période correspond aux nombres de couches électroniques occupées.
- 18 colonnes appelées FAMILLE et désignées de gauche à droite par un numéro de 1 à 8 ou par des chiffres romains suivis du symbole a ou b. La lettre b se réfère aux groupes des éléments de transition (éléments au centre du tableau).
Les éléments d'une même famille ont le même nombre d'électrons de valence :
- les éléments de la famille Ia ont 1 électron de valence ;
- les éléments de la famille IIa ont 2 électrons de valence ;
- les éléments de la famille IIIa ont 3 électrons de valence,...
Chaque colonne correspond à une famille d'éléments présentés dans des cases. Un nom est attribué à certains groupes (famille). Les éléments d'une même colonne ont tendance à avoir le même type de comportement (de réactivité).
nom des famille a :
· groupe 1 : Alcalins
· groupe 2 : Alcalino-terreux
· groupe (1)3 : Terreux
· groupe (1)4 : Carbonides
· groupe (1)5 : Azotides
· groupe (1)6 : Sulfurides
· groupe (1)7 : Halogènes
· groupe (1)8 : Gaz rares ou nobles
Le numéro des familles b a été choisi pour ses similitudes avec les numéros des familles a.
- Le tableau se compose horizontalement de 7 lignes. Elles sont appelées périodes et correspondent aux différentes couches présentées dans le modèle atomique de Bohr. Les périodes n'ont pas de nom spécifique, mise à part une portion de la période 6 (éléments 57 à 71) qui porte le nom de Lanthanides (nom tiré du premier élément de cette série) et les éléments 89 à 103 de la période 7 appelés Actinides (pour les mêmes raisons).
- 116 ÉLÉMENTS dont 90 naturels et 26 créés artificiellement, définis principalement par le symbole, le numéro atomique (Z) et la masse atomique de l'élément.
- 3 catégories d'éléments selon leurs propriétés : métaux, non-métaux, semi-métaux.
* La plupart des éléments sont des métaux.
* Les métaux sont donneurs d'électrons, les non-métaux sont accepteurs.
* Caractéristiques physiques des métaux : éclat métallique, conducteur de chaleur et d'électricité, malléable, ductile, solide à température ambiante (sauf Hg).
* Les semi-métaux ou métalloïdes : Nom désignant des éléments intermédiaires entre les métaux et les non-métaux.
Les métalloïdes sont difficiles à classer, ils sont à la frontière (ligne en escalier) qui sépare les métaux des non-métaux. Ils ressemblent aux non-métaux par certaines propriétés mais sont de faibles conducteurs en électricité (semi-conducteur). Ils sont à la fois donneur et accepteur d'électrons. (B, C, Si, Ge,...)
L'hydrogène est un cas particulier, il est tout seul, il n'appartient à aucune de ces trois catégories. Il a tendance à se comporter comme un métal dans certaines conditions et comme un non-métal dans d'autres conditions. Il peut-être donneur ou receveur d'électrons, il existe sous la forme neutre H₂, négative H⁻ ou positive H⁺.
- L'électronégativité :Le chiliste américain L. PAULING a calculé l'électronégativité des différents atomes.
Elle est notée : ℇ⁻ ou 𝒳⁻
Cette valeur reflète uniquement la tendance à attirer vers lui, à prendre des électrons. Cette valeur diminue lorsque le rayon atomique augmente (car diminution de l'attraction positive du noyau). Le tableau montre la variation de l'électronégativité des atomes qui augmente de gauche à droite dans les périodes et de bas en haut dans les familles. L'atome le plus électronégatif est donc l'atome de F (4.0) et les atomes les moins électronégatifs sont les atomes de césium et francium (0.7).
- Le tableau périodique nous permet de trouver facilement le nombre d'électrons de valence d'un élément. C'est très important car cela nous permettra de prévoir rapidement la charge de l'ion.
Chimiste russe, il proposa le premier en 1869 la classification la plus élaborée et la plus complète des 66 éléments chimiques connus à l'époque.
Il classa les éléments par ordre croissant de leur masse atomique en allant à la ligne de telle sorte que les atomes ayant des propriétés semblables se trouvent l'un en dessous de l'autre, formant ainsi une famille.
2. Structure générale
- 7 lignes appelées les 7 PÉRIODES
Le numéro de la période correspond aux nombres de couches électroniques occupées.
- 18 colonnes appelées FAMILLE et désignées de gauche à droite par un numéro de 1 à 8 ou par des chiffres romains suivis du symbole a ou b. La lettre b se réfère aux groupes des éléments de transition (éléments au centre du tableau).
Les éléments d'une même famille ont le même nombre d'électrons de valence :
- les éléments de la famille Ia ont 1 électron de valence ;
- les éléments de la famille IIa ont 2 électrons de valence ;
- les éléments de la famille IIIa ont 3 électrons de valence,...
Chaque colonne correspond à une famille d'éléments présentés dans des cases. Un nom est attribué à certains groupes (famille). Les éléments d'une même colonne ont tendance à avoir le même type de comportement (de réactivité).
nom des famille a :
· groupe 1 : Alcalins
· groupe 2 : Alcalino-terreux
· groupe (1)3 : Terreux
· groupe (1)4 : Carbonides
· groupe (1)5 : Azotides
· groupe (1)6 : Sulfurides
· groupe (1)7 : Halogènes
· groupe (1)8 : Gaz rares ou nobles
Le numéro des familles b a été choisi pour ses similitudes avec les numéros des familles a.
- Le tableau se compose horizontalement de 7 lignes. Elles sont appelées périodes et correspondent aux différentes couches présentées dans le modèle atomique de Bohr. Les périodes n'ont pas de nom spécifique, mise à part une portion de la période 6 (éléments 57 à 71) qui porte le nom de Lanthanides (nom tiré du premier élément de cette série) et les éléments 89 à 103 de la période 7 appelés Actinides (pour les mêmes raisons).
- 116 ÉLÉMENTS dont 90 naturels et 26 créés artificiellement, définis principalement par le symbole, le numéro atomique (Z) et la masse atomique de l'élément.
- 3 catégories d'éléments selon leurs propriétés : métaux, non-métaux, semi-métaux.
* La plupart des éléments sont des métaux.
* Les métaux sont donneurs d'électrons, les non-métaux sont accepteurs.
* Caractéristiques physiques des métaux : éclat métallique, conducteur de chaleur et d'électricité, malléable, ductile, solide à température ambiante (sauf Hg).
* Les semi-métaux ou métalloïdes : Nom désignant des éléments intermédiaires entre les métaux et les non-métaux.
Les métalloïdes sont difficiles à classer, ils sont à la frontière (ligne en escalier) qui sépare les métaux des non-métaux. Ils ressemblent aux non-métaux par certaines propriétés mais sont de faibles conducteurs en électricité (semi-conducteur). Ils sont à la fois donneur et accepteur d'électrons. (B, C, Si, Ge,...)
L'hydrogène est un cas particulier, il est tout seul, il n'appartient à aucune de ces trois catégories. Il a tendance à se comporter comme un métal dans certaines conditions et comme un non-métal dans d'autres conditions. Il peut-être donneur ou receveur d'électrons, il existe sous la forme neutre H₂, négative H⁻ ou positive H⁺.
- L'électronégativité :Le chiliste américain L. PAULING a calculé l'électronégativité des différents atomes.
Elle est notée : ℇ⁻ ou 𝒳⁻
Cette valeur reflète uniquement la tendance à attirer vers lui, à prendre des électrons. Cette valeur diminue lorsque le rayon atomique augmente (car diminution de l'attraction positive du noyau). Le tableau montre la variation de l'électronégativité des atomes qui augmente de gauche à droite dans les périodes et de bas en haut dans les familles. L'atome le plus électronégatif est donc l'atome de F (4.0) et les atomes les moins électronégatifs sont les atomes de césium et francium (0.7).
- Le tableau périodique nous permet de trouver facilement le nombre d'électrons de valence d'un élément. C'est très important car cela nous permettra de prévoir rapidement la charge de l'ion.
|
Numéro de la famille a
1 2 3 4 5 6 7 8 |
Nombre d'électrons de valence
1 électron 2 électrons 3 électrons 4 électrons 5 électrons 6 électrons 7 électrons 8 électrons |
Tendance
à perdre 1 électron à perdre 2 électrons à perdre 3 électrons à perdre ou à capter 4 électrons à capter 3 électrons à capter 2 électrons à capter 1 électrons Structure stable |
Ion formé
Cation de charge +1 Cation de charge +2 Cation de charge +3 Cation de charge +4 ou anion de charge -4 Anion de charge -3 Anion de charge -2 Anion de charge -1 Pas d'ion formé |
2. Les cases du tableau périodique
1. Légende

en haut à gauche : le numéro atomique
au milieu : le symbole de l'élément
en bas, centré : la masse atomique relative de l'élément
2. Le numéro atomique (Z) :
Dans le tableau périodique, on peut observer qu'un nombre est inscrit dans le coin supérieur gauche de la case. Il s'agit du numéro atomique Z de l'atome. Ce nombre indique l'ordre de classement de l'atome dans le tableau, mais aussi le nombre de protons (charges positives) de l'atome et par conséquent le nombre d'électrons (charges négatives) de celui-ci, car l'atome est électriquement neutre.
exemple : L'atome d'hydrogène a le numéro atomique 1, ce qui signifie qu'il est le premier atome par ordre de complexité, qu'il possède un proton dans son noyau et un électron périphérique.
3. La masse atomique relative :
Celle-ci est indiquée également dans le tableau périodique, elle se trouve en dessous du symbole de l'élément, ainsi la masse atomique relative (qui se note Ar) de l'atome d'hydrogène est Ar = 1,0079 d'après ce tableau.
EN BREF :
Que puis-je trouver comme informations principales sur le tableau périodique ?
* le nombre de protons : numéro atomique = Z
* le nombre d'électrons : numéro atomique = Z
* le nombre de nucléons : nombre de masse = A
* le nombre de neutrons = A - Z
* le nombre de couches occupées par les électrons = numéro de la période
* le nombre d'électrons de valence = numéro de la famille
* l'ion ou les ions formés
au milieu : le symbole de l'élément
en bas, centré : la masse atomique relative de l'élément
2. Le numéro atomique (Z) :
Dans le tableau périodique, on peut observer qu'un nombre est inscrit dans le coin supérieur gauche de la case. Il s'agit du numéro atomique Z de l'atome. Ce nombre indique l'ordre de classement de l'atome dans le tableau, mais aussi le nombre de protons (charges positives) de l'atome et par conséquent le nombre d'électrons (charges négatives) de celui-ci, car l'atome est électriquement neutre.
exemple : L'atome d'hydrogène a le numéro atomique 1, ce qui signifie qu'il est le premier atome par ordre de complexité, qu'il possède un proton dans son noyau et un électron périphérique.
3. La masse atomique relative :
Celle-ci est indiquée également dans le tableau périodique, elle se trouve en dessous du symbole de l'élément, ainsi la masse atomique relative (qui se note Ar) de l'atome d'hydrogène est Ar = 1,0079 d'après ce tableau.
EN BREF :
Que puis-je trouver comme informations principales sur le tableau périodique ?
* le nombre de protons : numéro atomique = Z
* le nombre d'électrons : numéro atomique = Z
* le nombre de nucléons : nombre de masse = A
* le nombre de neutrons = A - Z
* le nombre de couches occupées par les électrons = numéro de la période
* le nombre d'électrons de valence = numéro de la famille
* l'ion ou les ions formés