Ions
Dans un atome neutre, le nombre de protons = le nombre d'électrons.
Un ion, lui, est un atome ou une molécule ayant gagné ou perdu un ou plusieurs électrons.
Une perte d'électron(s) correspond à une charge globale positive : on parle d'un cation.
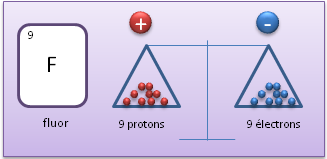
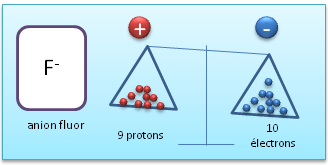
Un gain d'électron(s) correspond à une charge globale négative : on parle d'un anion.
Exemples :
Na → Na⁺ + e⁻
11p⁺ 11p⁺
11e⁻ 10e⁻
le cation Na⁺ a perdu 1 e⁻
O + 2 e⁻ → O²⁻
8p⁺ 8 p⁺
8e⁻ 10 e⁻
L'anion O²⁻ a gagné 2 e⁻
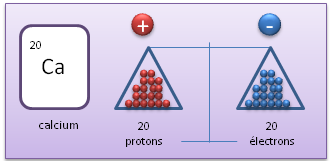
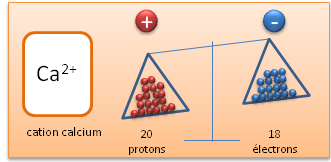
Ca Ca²⁺
20p⁺ 20p⁺
20e⁻ 18e⁻
1. Les espèces charges
I. Mise en evidence
Observe les étiquettes ci-dessous, repère les différents éléments présents dans cette eau.
Un ion, lui, est un atome ou une molécule ayant gagné ou perdu un ou plusieurs électrons.
Une perte d'électron(s) correspond à une charge globale positive : on parle d'un cation.
Un gain d'électron(s) correspond à une charge globale négative : on parle d'un anion.
Exemples :
Na → Na⁺ + e⁻
11p⁺ 11p⁺
11e⁻ 10e⁻
le cation Na⁺ a perdu 1 e⁻
O + 2 e⁻ → O²⁻
8p⁺ 8 p⁺
8e⁻ 10 e⁻
L'anion O²⁻ a gagné 2 e⁻
Ca Ca²⁺
20p⁺ 20p⁺
20e⁻ 18e⁻
1. Les espèces charges
I. Mise en evidence
Observe les étiquettes ci-dessous, repère les différents éléments présents dans cette eau.
Tu auras identifié plusieurs éléments chimiques et symboles déjà connus… Mais il y a une différence avec les symboles déjà vus !

À côté des symboles des éléments chimiques contenus dans cette eau, apparaît un signe mathématique en exposant (+ ou -). Cela signifie donc que ce ne sont pas les éléments neutres qui sont présents dans cette eau, mais des particules chargées qui ont les mêmes propriétés chimiques que les éléments neutres.
Nous avons déjà vu que dans un élément chimique, le nombre de protons (particules positives formant le noyau) et le nombre d'électrons (particules négatives gravitant autour du noyau) est identique. Dans les espèces chargées, les IONS, ces nombres de protons et d'électrons sont différents.
/!\ Les ions sont formés suite à un ajout ou un retrait d'électrons ! Les protons sont liés dans le noyau par des attractions très fortes et lorsque l'on forme un ion, on ne modifie JAMAIS le nombre de protons présents dans le noyau. (Pour rappel, c'est le nombre de protons contenus dans le noyau qui détermine l'élément !)
II. Expérience :
Regarder l’expérience ci-après : https://www.youtube.com/watch?v=UEi5mlzqZCU&feature=player_embedded
Nous avons observé qu'il a donc des espèces chargées dans l'eau. Montrons maintenant que ces ions sont de deux types : soit chargés positivement (plus de protons que d'électrons), soit négativement (plus d'électrons que de protons).
· Pour ce faire, nous allons faire passer un courant électrique dans une solution de CuSO₄ (sulfate de cuivre) et de K₂Cr₂O₇ (dichromate de potassium).
Dans un tube en U rempli d'une solution conductrice (H₂SO4 0,5 mol . L-1), l'on introduit le mélange d'ions et l'on place ensuite deux électrodes de graphite (carbone - comme la mine de ton crayon !). On fait passer un courant électrique dans la solution via les électrodes (une électrode est un matériau qui permet le passage du courant). Nous avons donc une électrode positive et une négative.
· Après 20 minutes, on observe que les ions se sont séparés aux deux électrodes. L'une montrant une couleur bleue, l'autre orange.
o Il y a donc bien deux types d'ions différents.
2. Définitions
I. Cation
Un cation est un ion chargé positivement, ce qui signifie que par rapport à l'atome neutre, il possède moins d'électrons.
Nous avons déjà vu que dans un élément chimique, le nombre de protons (particules positives formant le noyau) et le nombre d'électrons (particules négatives gravitant autour du noyau) est identique. Dans les espèces chargées, les IONS, ces nombres de protons et d'électrons sont différents.
/!\ Les ions sont formés suite à un ajout ou un retrait d'électrons ! Les protons sont liés dans le noyau par des attractions très fortes et lorsque l'on forme un ion, on ne modifie JAMAIS le nombre de protons présents dans le noyau. (Pour rappel, c'est le nombre de protons contenus dans le noyau qui détermine l'élément !)
II. Expérience :
Regarder l’expérience ci-après : https://www.youtube.com/watch?v=UEi5mlzqZCU&feature=player_embedded
Nous avons observé qu'il a donc des espèces chargées dans l'eau. Montrons maintenant que ces ions sont de deux types : soit chargés positivement (plus de protons que d'électrons), soit négativement (plus d'électrons que de protons).
· Pour ce faire, nous allons faire passer un courant électrique dans une solution de CuSO₄ (sulfate de cuivre) et de K₂Cr₂O₇ (dichromate de potassium).
Dans un tube en U rempli d'une solution conductrice (H₂SO4 0,5 mol . L-1), l'on introduit le mélange d'ions et l'on place ensuite deux électrodes de graphite (carbone - comme la mine de ton crayon !). On fait passer un courant électrique dans la solution via les électrodes (une électrode est un matériau qui permet le passage du courant). Nous avons donc une électrode positive et une négative.
· Après 20 minutes, on observe que les ions se sont séparés aux deux électrodes. L'une montrant une couleur bleue, l'autre orange.
o Il y a donc bien deux types d'ions différents.
2. Définitions
I. Cation
Un cation est un ion chargé positivement, ce qui signifie que par rapport à l'atome neutre, il possède moins d'électrons.
II. Anion
Un anion est un ion chargé négativement, ce qui signifie que par rapport à l'atome neutre, il possède plus d'électrons.
Un anion est un ion chargé négativement, ce qui signifie que par rapport à l'atome neutre, il possède plus d'électrons.
III. Ions polyatomiques - Ions composés
Un ion polyatomique est un ion constitué de plusieurs (poly) atomes. On parle aussi d'ion composé.
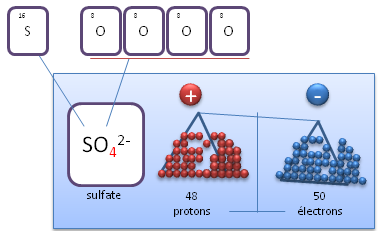
Le nombre de protons correspond à la somme des protons des atomes présents au sein de l'ion polyatomique et sa charge est définie par le nombre d'électrons total présents. Exemple : l'ion sulfate est chargé 2-, ce qui signifie qu'il possède deux électrons de plus que le nombre de protons total.
Un ion polyatomique est un ion constitué de plusieurs (poly) atomes. On parle aussi d'ion composé.
Le nombre de protons correspond à la somme des protons des atomes présents au sein de l'ion polyatomique et sa charge est définie par le nombre d'électrons total présents. Exemple : l'ion sulfate est chargé 2-, ce qui signifie qu'il possède deux électrons de plus que le nombre de protons total.
!!! À connaître !!!
OH⁻ ion hydroxyde
NO₃⁻ ion nitrate
SO₄²⁻ ion sulfate
CO₃²⁻ ion carbonate
PO₄³⁻ ion phosphate
NH₄⁺ ion ammonium
OH⁻ ion hydroxyde
NO₃⁻ ion nitrate
SO₄²⁻ ion sulfate
CO₃²⁻ ion carbonate
PO₄³⁻ ion phosphate
NH₄⁺ ion ammonium
Ionisation des atomes
1. Notion d’ion
Un atome électriquement neutre est un atome qui possède le même nombre d'électrons que de protons. Des charges ne peuvent apparaître que si le nombre de protons n'est plus égal au nombre d'électrons.
Le nombre de protons, contenus dans le noyau ne peut être modifié au cours d'un phénomène chimique non-nucléaire. C'est donc par conséquent les électrons qui jouent un grand rôle dans l'ionisation des atomes. Certains atomes ou groupements peuvent gagner ou perdre des électrons dans certaines situations.
définition: ion : substance chargée d'électricité car les charges positives et négatives ne se compensent plus complètement. Le noyau d'un ion simple est identique à celui de l'atome correspondant ; seul le nuage électronique est différent (le nombre d'électrons est différent).
2. Ion positif ou cation
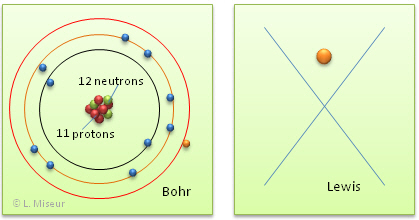
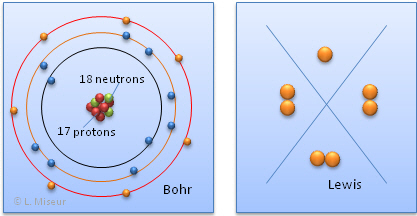
Représentons l'atome de sodium (Na) selon les modèles de Bohr et de Lewis :
Un atome électriquement neutre est un atome qui possède le même nombre d'électrons que de protons. Des charges ne peuvent apparaître que si le nombre de protons n'est plus égal au nombre d'électrons.
Le nombre de protons, contenus dans le noyau ne peut être modifié au cours d'un phénomène chimique non-nucléaire. C'est donc par conséquent les électrons qui jouent un grand rôle dans l'ionisation des atomes. Certains atomes ou groupements peuvent gagner ou perdre des électrons dans certaines situations.
définition: ion : substance chargée d'électricité car les charges positives et négatives ne se compensent plus complètement. Le noyau d'un ion simple est identique à celui de l'atome correspondant ; seul le nuage électronique est différent (le nombre d'électrons est différent).
2. Ion positif ou cation
Représentons l'atome de sodium (Na) selon les modèles de Bohr et de Lewis :
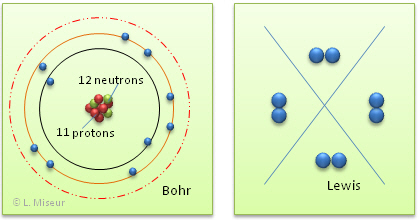
Tentons maintenant de représenter l'ion Na+, selon les mêmes modèles que précédemment.
L'ion Na+ a perdu son seul électron de valence, il possède maintenant une couche externe complète, il a la configuration d'un gaz rare (règle de l'octet). On peut représenter ce phénomène sous forme d'une équation :
Na ---> Na+ + 1 e-
De manière générale, les atomes ou groupements métalliques ont tendance à perdre leur(s) électron(s) pour atteindre la configuration d'un gaz rare.
atome --> ion positif + électron(s)
3. Ion négatif ou anion
C'est un atome qui est chargé négativement car son nombre de protons est inférieur à son nombre d'électrons.
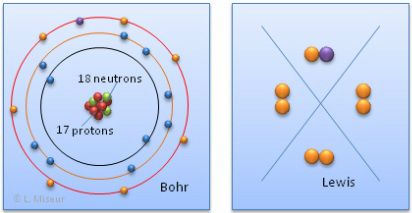
exemple : l'ion Cl- :
forme neutre (Cl)
Na ---> Na+ + 1 e-
De manière générale, les atomes ou groupements métalliques ont tendance à perdre leur(s) électron(s) pour atteindre la configuration d'un gaz rare.
atome --> ion positif + électron(s)
3. Ion négatif ou anion
C'est un atome qui est chargé négativement car son nombre de protons est inférieur à son nombre d'électrons.
exemple : l'ion Cl- :
forme neutre (Cl)
ion Cl-
Voici l'équation d'ionisation : Cl + 1e- --> Cl-
Forme générale : atome + électron(s) --> ion négatif
Note : L'équation d'ionisation d'un atome est TOUJOURS le nombre d'électrons à enlever ou à ajouter pour qu'il obtienne la configuration d'un gaz rare !
Remarque :
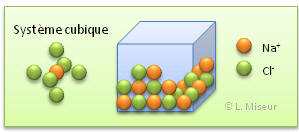
Des ions peuvent s'associer afin de former des solides. Ces solides sont alors composés d'ions positifs et négatifs qui s'attirent et se repoussent et ce jeu d'attraction-répulsion conduit à un arrangement particulier des ions en structures solides ordonnées.
Forme générale : atome + électron(s) --> ion négatif
Note : L'équation d'ionisation d'un atome est TOUJOURS le nombre d'électrons à enlever ou à ajouter pour qu'il obtienne la configuration d'un gaz rare !
Remarque :
Des ions peuvent s'associer afin de former des solides. Ces solides sont alors composés d'ions positifs et négatifs qui s'attirent et se repoussent et ce jeu d'attraction-répulsion conduit à un arrangement particulier des ions en structures solides ordonnées.